どうもこんにちは、だいさくです。
先日サンバイオの記事を書いたんですが、
サンバイオがSB623で立ち上げ準備!情報まとめ、これは要チェック!
この記事を書いたことがきっかけで 、
再生医療について勉強してみました。
2012年に京都大学の山中教授がiPS細胞、
「成熟細胞が初期化され多能性をもつことの発見」
によってノーベル生理学・医学賞を受賞してから、
製薬会社の界隈でも次の波は再生医療だ!みたいなことは言われてたんですが、
いよいよ本格的な再生医療の時代に入ったと言えそうです。
これは恐らくオンコロジー領域の分子標的につぐ大きな波は、
再生医療で間違いなさそうです。
ここ何日間か会社から帰宅後はずっと再生医療について勉強してたので、
今日は勉強したことのまとめ的な感じで書いて行きたいと思います。
再生医療とは何か?
再生医療とは何か?ということですが、厚生労働省の定義では以下の2つです。
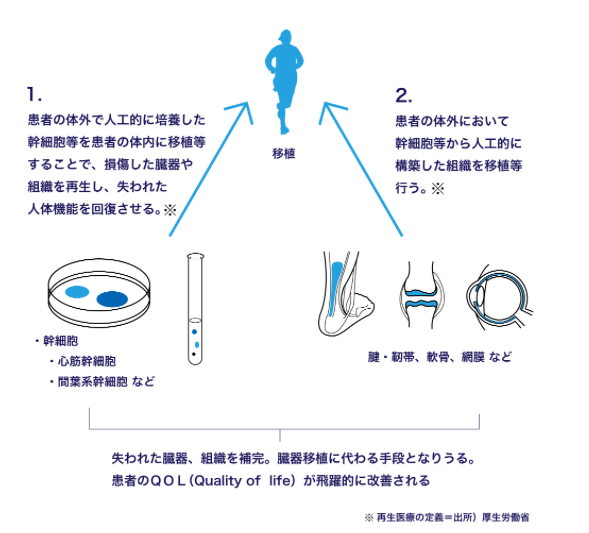
①患者の体外で人工的に培養した幹細胞等を患者の体内に移植等をすることで、損傷した臓器や組織を再生し、失われた人体機能を回復させる。
②患者の体外において、幹細胞等から人工的に構築した組織の移植等行う。
この二つです。
私の調べた限りですと、
幹細胞は自家(患者本人)を使用したものと他家(患者以外)を使用したものに分けられますが、間葉系幹細胞の治療は他家を使用したもの、いわゆるCAR-Tなどの遺伝子治療は自家を使用したものが主流ではないかと考えられます。
現在臨床に応用が可能なものは間葉系幹細胞を培養した治療法、そして遺伝子治療の分野に関しては臨床化が進んでいると思います。iPSが遅れ気味です。(理由は後述)
再生医療とは、生まれつきもしくは不慮の事故や疾病、加齢に伴い、欠損・損傷・機能低下した組織や臓器を上記の方法培養した細胞や組織を用いて修復再生し、機能を補完する医療のことを言います。
欠損や損傷した臓器を再建させることで、疾病や損傷への根治的治療が可能となり、患者さんや高齢者、障害者の生活の質QOLが飛躍的に向上し、社会復帰と生活自立が可能となります。このことにより医療分野だけでなく、産業の構造や社会構造の変化をもたらすことが期待されています。
再生医療は今までの治療と何が違うか?

再生医療は今までの治療と何が違うのでしょうか?
1番の違いは継続的な治療が必要ないというところです。
例えば、人工透析やペースメーカを使用してる患者さんであれば、
対症療法として投薬や医療機器にずっと依存する生活をしなければなりません。
しかし、再生医療は自家、もしくは他家の幹細胞を培養し、
患者さんに移植することで、
元々持ってる人体機能そのものを回復させます。
治療が1回で済みますし、疾患によっては根治的な治療が可能になります。
例えばサンバイオのSB623が2020年頃に日本での上市がされそうですが、
外傷性脳損傷で寝たきりになっていた患者さんは、
起き上がり自分のことは自分でできるようになった、
腕が上がるようになった、
言語障害が改善されたといった結果が出てます。
そのことにより改善されたのは患者さんのQOLだけでなく、
それを介護するご家族のQOLも改善されます。
そう言った意味も含めて、社会構造に変化が起きると言われています。
再生医療はiPSより間葉系幹細胞が主流
再生医療の分野は日本は比較的先を走っていると思います。
サンバイオのSB623もニプロのステミラック注にしても日本が先駆けて承認されます。
それだけ再生医療の分野が注目され、
これだけ早く製剤化されたのは、
山中教授がノーベル賞を取ったことで、
強い注目を浴び、製薬会社からも投資が集まったことが大きな要因だと思います。
ただ、現在の開発状況などを見ていると、
iPS細胞よりは「間葉系幹細胞」です。
「間葉系幹細胞」これは再生医療を考える上で、
結構重要なキーワードになると思います。
再生医療のキーワード間葉系幹細胞とは?
※写真はイメージです
上述の2社サンバイオとニプロの再生医療に関する報道で
「間葉系幹細胞」にかなり注目が集まっています。
間葉系幹細胞は人の骨髄や脂肪、臍帯などに含まれており、
骨や脂肪、神経などに分化する働きを持つ細胞です。
iPS細胞やES細胞などあらゆる細胞に変化する能力を持つ「万能細胞」とは異なり、
比較的容易に採取することがでいる他、
細胞のがん化リスクが低いとされています。
そのため上述した②番のパターンで活用されるケースが多く、
実際にサンバイオ、ニプロの両社でも間葉系幹細胞を培養して
今回の結果が得られております。
また、他家のiPS細胞を移植すると拒絶反応が起き、
通常の造血幹細胞移植同様に免疫抑制剤が必要になるそうです。
しかし、間葉系幹細胞は他家のものを使用しても拒絶反応が起きません。
そう言った安全性の違いに関しても現状では間葉系幹細胞の方が有利であると考えられます。
再生医療のリスク
再生医療と言っても再生細胞治療や遺伝子治療がありますが、
一般的に言われている再生医療のリスクとして、
・特に自家細胞の培養ケースは効果にバラツキが生じる
・他家細胞の培養ケースは拒絶反応が見られる事がある
・薬価が高額である
・患者が限定的であることが多い
この4つが一般的に言われております。
日本で上市(済)される予定再生医療製剤
現在日本で上市が決まっている、
もしくは上市が見込まれている再生医療製品を現段階のものをまとめます。
| 販売会社 | 製剤 | 適応 | 承認日 (予定) |
備考 |
| JCRファーマ | テムセルHS注 | 急性GVHD治療 | 2015年9月 | 間葉系幹細胞(希少疾患) |
| テルモ株式会社 | ハートシート | 標準治療で効果不十分な虚血性心疾患による重症心不全治療 | 2015年9月 | ヒト骨格筋由来細胞製品 |
| ノバルティス | キムリア (CTL019) |
B細胞性急性リンパ芽球性白血病/びまん性大細胞型B細胞リンパ腫 | 早ければ 2018年中 |
T細胞遺伝子改変 |
| ニプロ | ステミラック注 | 脊髄損傷 | 早ければ 2018年中 |
間葉系幹細胞 |
| サンバイオ | SB623 (開発コード) |
外傷性脳損傷 | 早ければ 2019年末頃 |
間葉系幹細胞 |
| ノバルティス | AVXS-101 (開発コード) |
脊髄性筋萎縮症(SMA) | 早ければ 2019年中 |
遺伝子治療 (薬価4億5千万) |
現在の再生医療の開発状況
こちらは現在の再生医療製剤に関する開発状況になります。
開発状況は基礎研究のものも含めると相当の数になりますので、
主要なものだけ記載していきます。
特にiPSに関してはほとんどが基礎研究段階になっておりますので、
臨床に近い段階のみ記載してます。
| 会社名 | 製品名 | 細胞 | 適応 | 日本の現状 | 備考 |
| 第一三共 | KTE-C19 | T細胞CAR | 大細胞型B細胞リンパ腫 | P2 | 米国承認済み |
| セルジーン | JCAR017 | T細胞CAR | 非ホジキンリンパ腫 | P2 | |
| タカラバイオ | TBI-1501 | T細胞CAR | 急性リンパ芽球性白血病 | P1/2 | 販売は大塚製薬 |
| タカラバイオ | NY-ESO-1・siTCR | T細胞CAR | 滑膜肉腫 | P1/2 | 販売は大塚製薬 |
| JRM (ノーリツ鋼機) |
JRM-001 | 自家心臓細胞 | 小児先天性心疾患 | 臨床試験 | 20年上市予定 |
| 大塚製薬 | MMG49/CAR-T | T細胞CAR | 多発性骨髄腫 | 基礎研究 | 大塚/大阪大学 |
| セルシード | CLS2702C/D | 自家表皮 | 食道がん後狭窄 | P3 | 先駆け審査 |
| ムンディファーマ | Invossa | 他家軟骨 | 変形性膝関節症 | 臨床試験予定 | 韓国承認済み |
| ヘリオス | HLCM051 | 間葉系幹細胞(骨髄) | 急性脳梗塞 | P2/3 | |
| サンバイオ | SB623 | 間葉系幹細胞(骨髄) | 慢性期脳梗塞 | 米国にてP2b | |
| 三菱ケミカルHD | CL2020 | 間葉系幹細胞(骨髄) | 心筋梗塞 | 探索的臨床試験 | |
| 三菱ケミカルHD | CL2020 | 間葉系幹細胞(骨髄) | 亜急性期脳梗塞 | 探索的臨床試験 | |
| 武田薬品 | Alofisel | 間葉系幹細胞(脂肪) | クローン病に伴う肛門複雑瘻孔 | 未定 | 欧州承認済み |
| ロート製薬 | ADR-001 | 間葉系幹細胞(脂肪) | 肝硬変 | P1/2 | |
| Regeneus | Progenza | 間葉系幹細胞(脂肪) | 骨関節炎 | 未定 | 豪でP1完了 |
| リプロセル | Stemchemal | 間葉系幹細胞(脂肪) | 脊髄小脳変性症 | 前臨床 | 治験計画届出 |
| ツーセル | gMSC1 | 間葉系幹細胞(滑膜) | 膝軟骨損傷 | P3 | 20年上市 |
| ツーセル | gMSC1 | 間葉系幹細胞(滑膜) | 中枢神経領域 | 基礎研究 | |
| 帝人/JCR | JTR-161 | 間葉系幹細胞(歯髄) | 慢性期脳梗塞 | 基礎研究 | |
| CYNATA | CYP-001 | 間葉系幹細胞(iPS) | GVHD | 未定 | 海外P1進行中 |
| 第一三共 | / | iPS | 心不全 | 試験準備中 | 22年上市目指す |
| iHeart Japan | IHJ-301 | iPS | 重症心不全 | 基礎研究 | 21年臨床開始 |
| 小野薬品 | / | iPS(CAR-T) | がん | 基礎研究 | |
| 大塚製薬 | / | iPS | 血小板製剤 | 基礎研究 |
製薬会社の次の波は再生医療で間違いない!

今回のサンバイオ、そしてニプロの再生医療に続いて、
おそらく今後、間葉系幹細胞に関する製剤が上市のラッシュになるのではないかと思います。
再生医療は今までしっかりとした治療法がなかった疾患に対する臨床試験が多いです。
製薬企業の当たり前の戦略として、
まずは治療法の少ない希少疾患から始めるというのがありますが、
再生医療が今後どのような方向になるかはわかりませんが、
まずは希少疾患から適応になっていくと思います。
今回情報をまとめていて感じたことは、
臨床試験で対照となる薬剤や治療法がない疾患が多く、
安全性が担保され、それなりの結果を出せば、
承認にされやすいのではないかと感じました。
これが今から10年後くらいになったら今のオンコロジーのように群雄割拠に
なることはあり得ると思いますが、
とにかく今、そしてこれからは、
再生医療と希少疾患の本格的な時代に入ると考えてもおかしくないと思います。
再生医療の市場は大きい!
再生医療は現在では希少疾患や一部の慢性疾患に適応となっておりますが、
経済産業省の報告では、
再生医療産業の日本国内市場規模は、
2012年の段階では100億円程度でしたが、
2020年に950億円、
2030年に1兆円、
世界的にも2030年に5.2兆円まで拡大すると言われています。
医薬品の市場で1兆円は現在の抗がん剤の市場(2017年が1兆1千億)と同程度です。
100億円程度の市場が10年後に1兆円市場というのは
やはりこぞって開発費が注がれるのも理解できます。
再生医療領域に求められるスキルは?
再生医療領域の分野が今後どんどん立ち上がると考え、
求められるスキルはどういうものかなと推敲すると、
血液領域のスキル、
特に造血幹細胞移植の領域は比較的精通されるんではないかと感じました。
ただ、間葉系幹細胞の培養の場合は拒絶反応が見られないようなので、
単純に適応になるその疾患に対しての知識が重要ではないかと思いました。
オンコロジーとかプライマリーとかは全く関係ないと思います。
投薬を続けるわけではなく、
1回の治療で終わるのでどちらかというとイメージ的には、
やはり造血幹細胞移植に似てるのかなと思いました。
またチーム医療も必要になってくると思います。
最後に
ここ数日間で勉強した再生医療に関して情報をまとめて見ました。
再生医療には相当な投資が注がれており、
日本だけで臨床試験が完結できるような患者数の多い疾患にも臨床試験が
走っているのは、オンコロジー領域などと異なってやりやすい部分かなと感じます。
MR目線として今後何が来るか?どんな大きい波が来るか?
という目線は絶対に必要だと思います。
今後は10年くらいは希少疾患と再生医療で大方はずれてはないとおもいます。
ご参考になれば幸いです。
ではまた!



コメント