どうもこんにちは、だいさくです。
アデュカヌマブが未だ世間を騒がせていますね。
私も以前記事を書かせていただいたんですが、
アデュカヌマブ何故承認!?胡散臭い薬と言われる理由をまとめてみる
この記事ツイッターにアップした事もあって、非常に沢山読んでいただいた事はとても嬉しい反面、
反省してる点として、アデュカヌマブが悪いというわけではなく、
この薬を承認した一連の動きが、「怪しい」「胡散臭い」っていう事なんですよね。
もっとそう言った書き方をするべきだったと反省しております。
僕の記事では有効性が現状不明にも関わらず、
副作用は確実に(しかも結構)出るこの薬に年間600万円もかかってしまう、
そしていわゆるフェーズ4(市販後臨床試験)で有効性を確認していく事が、
ただの人体実験であるように感じる事、
そのフェーズ4の結果が出るのがなんと8年後という部分に、
胡散臭さを感じてしょうがないと書きました。
ただ、それからも本当に沢山のメディアでアデュカヌマブ批判が繰り広げられていた訳ですが、
実は今回の承認劇をきっかけにCNS全盛時代がくる予感がしています。
今回のアデュカヌマブの承認劇を経て米イーライリリー社のdonanemabが、
新たな指標を持って承認になる可能性も出てきたのでその辺も少しご注目いただきたいというか、
混沌としていた今後のCNS領域の方向性も見えてくるのかなと感じました。
アデュカヌマブの承認によってCNS領域全盛時代がマジでくるかも!
ちなみに僕の記事にいただいたコメントとして、
「画期的な作用機序を有してる薬が承認された事で患者さんの選択肢が増える事は単純に喜ばしい事では?」というコメントをいただいたのですが、
気持ちは大変わかりますし、確かに患者支援団体は喜んでいるみたいなんですよね。
でもやっぱりそれは違うと言いますか、
選択肢が増えてしまうこと自体がダメなんですよね。
有効性が不明で副作用が確実に出る薬が選択肢に入ってしまうから良くないんですよ。
だって使いたくなっちゃうじゃないですか。保険の範囲内に入ってしまえば。
特に日本は民間の医療保険では無いわけで、承認されていれば使えてしまうわけで、
だからもしかしたら効くかも?と思って使えてしまうわけですよ。
その選択肢に入ってしまうことが良くない事だと思うわけです。
ちなみに、僕が記事を書いてからも米国のICERという医療経済を評価する機関も、
「アデュカヌマブは健康への真の利益なし」という長々として発表をしておりますし、
Bloombergからも、
「バイオジェンのアデュカヌマブを米国の主要医療センターが投与しない方針」
バイオジェンのアデュカヌマブ、米主要医療センターが投与しない方針
という記事を出していて、
一部の保険会社も一切この薬の保険を認めないとされています。
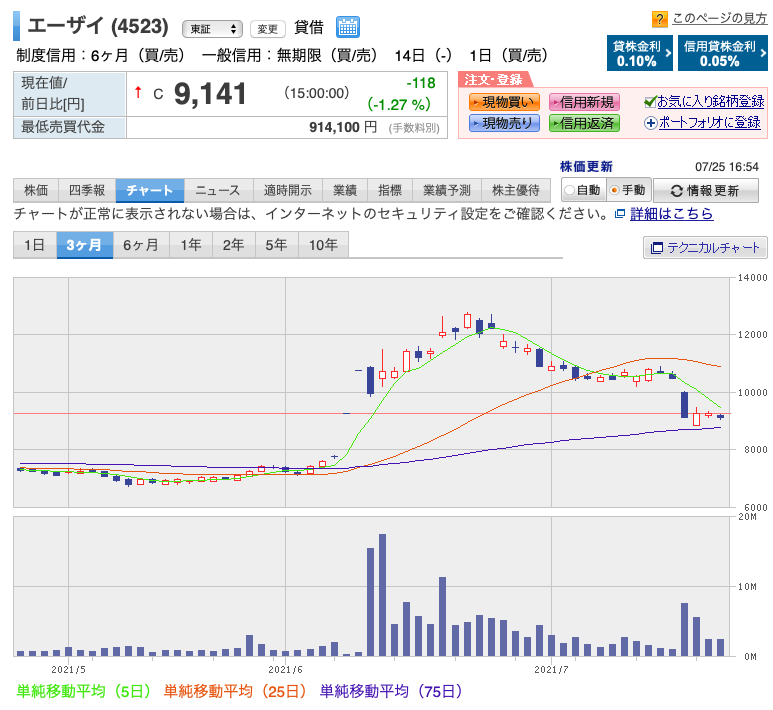
ちなみにその「米国で使わない」報道がされて以降、
バイオジェンもエーザイも株価は当初から上がった分の4分3くらいはまた下がりました。
また、FDAの承認プロセスに関してかなり怪しいという事で、
米国の連邦機関が独立した立場から調査することも決定してます。
ということでここまででかなり怪しい承認プロセスを経ている、
という事をお伝えさせていただきましたので、
ここからは肯定的にアデュカヌマブについて書いていきたいと思います。
アデュカヌマブは既に投与されている

アデュカヌマブですが、米国の不動産業を営む方に投与がされており、
その後ももちろん適応通り超早期のMCI患者に対して投与がされております。
FDAの承認プロセスが怪しかろうが承認はされているわけで、
保険適応を拒否していない保険会社も当然存在しているので、
あくまで臨床試験の一環として投与がされております。
バイオジェンの決算でどれだけの売り上げがあるかという所が興味深いところですが、
兎にも角にもアデュカヌマブを欲してる患者に投与ができる、
そして処方をする医師も一定数以上はいるということになります。
アデュカヌマブは確実にAβ量を減少させている

Aβ(アミロイドベータ)タンパク質の量が増える(蓄積)ことが、
アルツハイマー型認知症の発病の要、引き金を引くという意味のトリガーと言われております。
このAβと言われる異常なタンパク質が脳内に蓄積されることがきっかけで、
この病気の引き金を引くことが明らかになってきているのですが、
アデュカヌマブはこのAβの量を確実に減少させています。
承認のきっかけとなった2つの第3相試験のEMERGE試験では71%、
そしてENGAGE試験では59%で減少が確認されてます。
これはアミロイドPET検査によって測定をしておりますが、

いやいや、それが臨床的に有効性を示せてないんだからダメでしょ!
と、考えてしまうわけですが、
高用量では有効性が確認されているのです。(あくまで後ろ向きですが)
んで、2つの試験では、
ARIA-E(脳内に対する副作用)が高用量にすると強く出るという懸念がある事から、
高用量投与群が選ばれにくかったこと、
そして特にENGAGE試験では、
rapido progressorというアデュカヌマブが効きにくい病性進行が早い患者が多く含まれていた事で、
全体の有意差が確認できなかったですが、
当初言われていた高用量で病性進行の遅い早期患者にはしっかり有効性は確認できたという訳になります。
ただ、2019年に「無益性」が発表され試験中止になったこともあり、
レトロ解析(後ろ向き)だけで承認するというのは中々どうして批判を浴びてしまうんだと思います。
FDAの諮問委員には認知症の専門医がいなかった
今回のFDAの諮問委員に認知症の専門医がいなかったことを指摘している、
日本のお医者さんがいらっしゃいました。
日本の治験にも入られている施設のお医者さんだったんですが、
今回の諮問委員のメンバーは公衆衛生学や薬剤の疫学を担当している専門家など、
様々なメンバーが含まれていますが特にアルツハイマー病の専門家はほとんどいなかったようです。
そのためAβ減少の有用性や、高用量とMCI患者に対する有効性を正しく評価してないのでは?
迅速承認制度の適用の妥当性について議論されていないという指摘がありました。
僕は癌のことしかわかりませんが、癌の諮問医院でも実は専門家ってほとんどいないんです。
外部や他の領域の専門家が集まってそれを正しく評価するのがFDAの諮問会議なので、
何故わざわざ今回に限って専門家を用意する必要があるのかはちょっとわからないですが、
とにかく今回の迅速承認についてはアルツハイマーの専門家はいませんでした。
アルツハイマーの有効性の指標が変わる可能性

アルツハイマーの有効性に関する指標が今回の承認劇をきっかけとして変わっていく可能性があるようです。
例えば早期の癌でも自覚症状が全くなくてもそこに癌があれば治療を行います。
手術したりして癌を取り除く訳ですが、癌による自覚症状がなくても、
それを取ること、治療をすることで何かしらの後遺症や痛みは当然ある訳です。
今回のアルツハイマーでも超早期の患者に投与を行うことによって、
タウの蓄積量を抑えてるとか、Aβ量を低下させたというのが、
その後の発症を遅らせたりする効果につながると考えられて、
指標をそういったある意味予防の方にシフトしていく可能性があります。
CNS領域全盛時代がくる?イーライリリーのdonanemabとは?
Donanemab in Early Alzheimer’s Disease
今回のアデュカヌマブのP4でもPET測定することで有効性を確認したり、
現在米イーライリリー社が行っているdonanemab(抗Aβ抗体)の臨床試験でも、
PETで測定したAβの量が正常レベルにまで減少させることと、
ある程度の臨床効果が確認されたら、
あとは休薬するというスキームになっています。
正直この流れは認知症治療薬を承認するにあたって非常にハードルが低くなります。
ちなみにイーライリリーは2021年度中にFDAに申請をすると表明しています。
最後に
ちょっと色々方向性が飛んでしまいましたが、
アデュカヌマブが曰く付きの承認をされたことによって、
認知症の臨床試験のあり方に変化が起こりそうであるということ、
まだまだ重度の認知症治療の根本治療は難しそうですが、
MCIなどの早期の患者には逆にどんどん治療薬が出てくる可能性があるのかと思いました。
イーライリリー社も今回のアデュカヌマブの承認を見て方向性を変えてきているようなので、
根本治療にはまだつながらないですが、
CNS領域の夜明けを感じるような一つの小さな光があるのかなぁと思いました。
ではまた!



コメント