どうもこんにちは、だいさくです。
米国のインスメッド社が日本に参入してくるとの情報を頂戴することができまして、
今日はインスメッド社について、
そしてインスメッド社が手がけるArikayce(アリケイス)について、
情報をまとめてみました。
あくまで個人的な感想ですが、
アルナイラム以来の面白そうな案件な気はしております。
アルナイラムもプライマリー系の方が重宝されてましたが、
インスメッドもプライマリー系の経験者の方が優遇されそうです。
日本から発信されている情報があまりなかったので、
細かい部分も書いており、かなり長い記事になってしまいましたが、
ご興味ある方是非チェックしてみていただければと思います。
米インスメッド日本参入!転職情報やArikayceについてまとめる!
Arikayce(アリケイス)は、アミカシンリポソーム吸入懸濁液で、
肺MAC症に使用する吸入型の新薬になります。
2018年9月18日にFDAで承認され、日本では恐らく2021年頃を目処に発売されます。
細かい事は後述しますが、日本の適応は恐らく、
「一般的な抗生剤の既治療例で難治性の肺MAC症」になるのではないかと思います。
肺MAC症患者は世界では日本が一番罹患数が多いため会社としても力を入れています。
現在立ち上げメンバーを募集しており、
とにかくこの記事は長いので、募集要項を始めにお示します。
インスメッド(Insmed)合同会社についてと募集要項

インスメッドは2020年1月現在の段階で、日本のHPもまだ無いです。
日本ではインスメッド合同会社という名前で、東京の永田町に本社があり、
現在社員は11名となっています。
日本法人の社長は折原祐治社長で、元ギリアド日本法人の社長をされていた方です。
元々アムジェンの社長も歴任されていますよね。

※ギリアド時代の折原祐治社長
折原さんはギリアドの日本立ち上げを担い、
ハーボニー、ソバルディ、ベムリディの3製品を上市させ、
ご存知の通りギリアドを日本で大成功させた功労者です。
僕はハーボニーの偽造薬流通問題の時に陣頭指揮を取られていたのが記憶にあります。
ギリアドを辞める時(2017年末頃)が64歳くらいで、
「僕はもう引退」みたいな事を仰っててギリアドのアドバイザーみたいな仕事されてたんですが、
インスメッドの社長になられてました。
インスメッドの募集要項
インスメッドは既にメディカル部門やマーケティング部門など営業部門の他に、
サプライチェーンなど自販体制に関する整備が進められています。
募集要項は職種によって様々ですが、
営業部門に関しては、
・MRとして高い成果をあげて表彰を受けた経験
・大学病院など基幹病院において新薬の採用経験
・呼吸器疾患、または感染症領域、希少疾患やオンコロジー領域、あるいは少数精鋭組織での営業経験があればなお可
この辺が必須になります。
扱うのが肺MAC症で、基本的には呼吸器内科、感染症内科に出入りするので、
その辺の経験がある方や、非喫煙者とされてます。
あとは、すべての職種の募集要項に書いてあるのが、
「希少疾患に本気で向き合いたい方」と書かれてあります。
立ち上げ系とか小さいバイオベンチャーの会社は総じて情熱が重視されますので、
しっかり勉強してパッションを整理しておいた方が良いと思います。
想定年収はあくまで前職考慮とされてますが、
記載されているのは1000万〜1800万となってます。
また米国で上場しているのでストックオプションもつくかもしれませんね。
そこまで株価高く無いのでRSUもらって、日本で成功して、上がったらメッチャ良いですね。
あと、福利厚生などの細かい情報はわからないですが、
退職金も有りとなっています。
面接は2回〜、多分ですが英文レジュメが必要で、英語面接もありそうです。
案件はランスタッドが持ってます。
特に営業部門は英語に関してはそこまで高いものを求められてません。
東大生の英語より、大阪のおばちゃんのジェスチャーの方が外国人に伝わりやすいと、
言われているのと同じで、
私は英語無理〜と諦めるとチャンスのほとんどの選択肢を無くしてしまうので、
身振り手振りでもなんでも良いから伝えてみると良いと思います!
(とにかく英語ぐらいで諦めないでと言いたい!)
日本における肺MAC症の想定患者数

冒頭でも肺MAC症は日本が一番市場が大きいとお伝えしましたが、
肺MAC症は簡単に言うとMAC菌が原因の感染症です。
日本での想定患者数はどれくらいか?というところですが、
肺MAC症は、肺NTM症(非結核性抗酸菌症)の中の一つで、
肺NTM症の約88%が肺MAC症になります。
2014年にAMEDが実施した、日本呼吸器学会認定施設、及び関連施設884施設の調査によると、
肺NTM症の罹患率は14.7/10万人ですので、
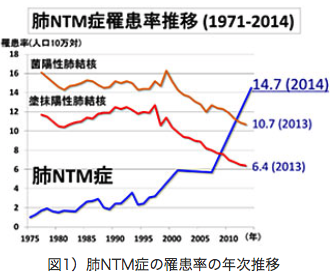
大体15,240人になり、その88%13,411人が肺MAC症となります。
この罹患数は世界でトップとなっており、
FDAの承認のきっかけとなったピボタル試験にも日本の施設がエントリーされ、
日本への期待が大きいことがわかります。
ちなみに西日本に患者が多い傾向がありそうです。
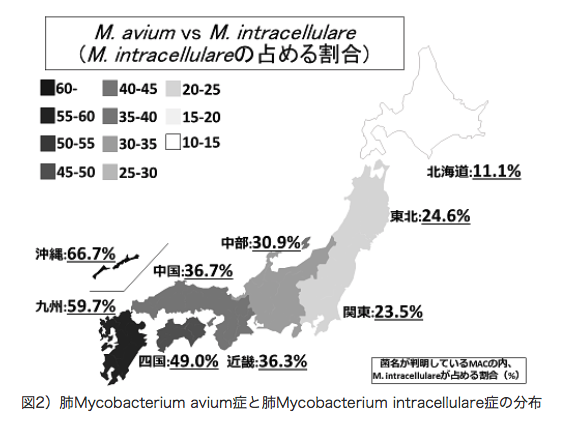
Arikayceの適応が日本でどうなるかわかりませんが、
難治性の肺MAC症になると予想されますので、
恐らく対象患者は少なく見積もって肺MAC症全体の30%程度で、約4000人くらいかと思います。
大体年間1000人程度の患者さんがこの疾患でなくなっているようですが、
基本的には死に直結するような疾患ではなさそうです。
インスメッドがどれくらいの規模の営業体制を考えているのかはちょっと今の所わからないですが、
新規患者が少なく見て年間4000人というのは、言葉は適切でないかもしれませんが、
希少疾患領域としてはちょうど良いやりやすい人数かと思います。
年間200人とかだと本当に患者さんが全然いないので、逆に大変かもしれません。
むしろ昨今の状況を考えると、希少疾患といっても規模は十分なので、
呼吸器系を手掛ける会社だったら喉から手が出るくらい欲しい薬剤では無いかと思います。
※ただ、これは諸説あって、あくまで患者数は少なく見積もってます。少し前のデータですと、この倍以上患者がいるというデータもあります。
肺MAC菌とは?
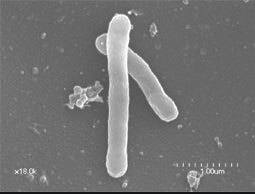
※MAC菌
ではArikayceが適応となる肺MAC症の原因となる肺MAC菌とはなんでしょうか?
肺MAC(Mycobacteria.avium complex)は上述の通り、
肺NTM(nontuberculous mycobacteria;NTM)の中の一種で、
肺NTMというのは非結核性抗酸菌ですが、
結核菌と特殊栄養要求菌を除いた菌群の総称が肺NTMになります。
日本では30種類以上の菌種による感染症が報告されておりますが、
その中でも一番多いのが肺MAC菌(80〜90%)と言われています。
基本的に自然界の土壌、水系、都市の給水システムなどに生息する環境生息菌であるが、
人から人への感染は否定されています。
浴室で感染しやすいとも言われており、
昨今罹患率が急増していると言われている要因が、
風呂場での感染で、42度前後の温度で繁殖しやすく、MAC菌にとってまさに最適な環境のようです。
浴槽のお湯の注ぎ口、シャワーヘッドのぬめりや湯あかにいて、
そうした場で霧状の水滴やホコリが発生すると、
MAC菌を肺に吸い込み感染しやすいのでは?とのことです。
日本の罹患率が高いのはお風呂好きだからなんでしょうかね。
しかもお風呂洗いをよくする人(疫学では40歳以上の主婦に多い)が罹患しやすいようですので、
昔はお風呂毎日洗わない家も多かったみたいですが、(実家もそうでした)
昨今お風呂を毎日洗う綺麗好きな人が増えたからとかも理由なんでしょうかね。
肺MAC症に関しては、複十字病院のサイトがとてもわかりやすいです。

複十字病院は治験にもエントリーされていて、
尾形先生はオピニオンの一人では無いかと思います。
Arikayceとは?
それでは、このArikayce(アリケイス)とはどんな薬剤なのか?と言うところですが、
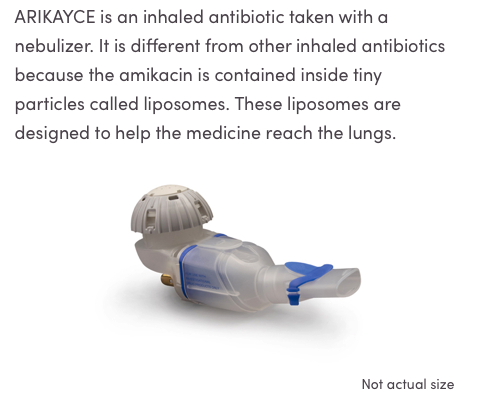
アリケイスは、
アミカシンという抗生物質をリポソームさせ、ネブライザーで摂取する吸入剤になります。
正式名称はAmikacin Liposome Inhalation Suspension(ALIS)で、
治験ではALISと称されています。
アミカシンは、元々静脈内投与される強力な抗マイコバクテリア剤ですが、腎毒性や聴覚毒性が強くでます。それを吸入送達用のリポソームにカプセル化した硫酸アミカシンがアリケイスになります。
これにより有効性を担保し安全性を改善されたようです。
アミカシンは元々通常の抗生物質より強い作用が元々あるが、普通に投与すると使いづらいため、改良したのがアリケイスであるという感じでしょうか。
Arikayceは売れるのか?①
実際このArikayceは売れるのか?と言うところですが、
こちらがP3試験の6ヶ月時点での論文になります。タイトルにもありますが、CONVERT試験と呼ばれていて、P3試験にこのような名前が付けられるのは大抵企業がバックにいる事が多いため、ピボタル試験と捉えて良いと思います。ただ最終解析の論文はpubmedでは見つけられませんでした。(まだ出てない可能性が高いと思います)
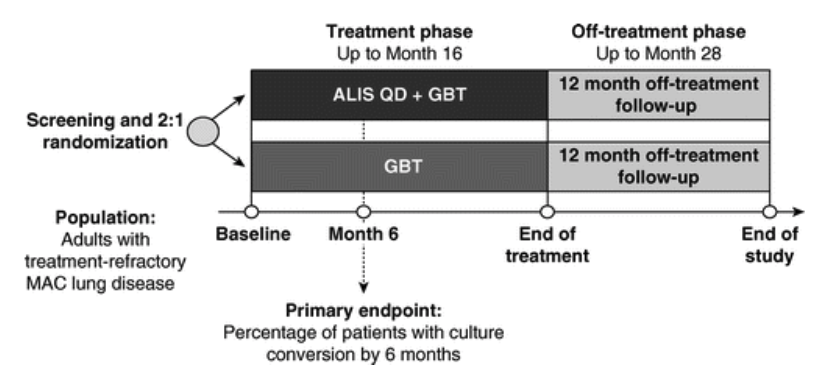
上記の表が試験デザインで、GBTというのは、ガイドラインベースの治療になります。
※肺MAC症は一般的に、複数の抗生剤などを用いた薬物療法が行われますが、これが有効!と言うのは現在明確にはわかってません。ガイドライン上でも実臨床でも代表的な治療薬はクラリスロマイシン(CAM)とエタンブトール(EB)ですが、そのほかに、リファンピシン(RFP)を加えた3種類での治療がメインになります。また病状によって、ストレプトマイシン(SM)、カナマイシン(KM)など注射剤を使用し、複数の治療薬を投与して「数打ちゃ何か当たる戦略」が取られております。アリケイスはこういった治療に反応しない患者が対象となってます。なので今回のGBTに関しては標準治療抵抗性なので、非経口抗生物質投与がガイドラインで設定されておりますので、その辺が対象になっています。ただ、多くの場合が失敗するので、改善が必要だとこの論文の前提の部分で書かれております。
その改善が必要なGBT群にALIS(アリケイスのこと)を加えた群で比較したP3試験がCONVERT試験になります。ちなみに、GBT単独群にもしっかりALISのプラセボが投与されています。
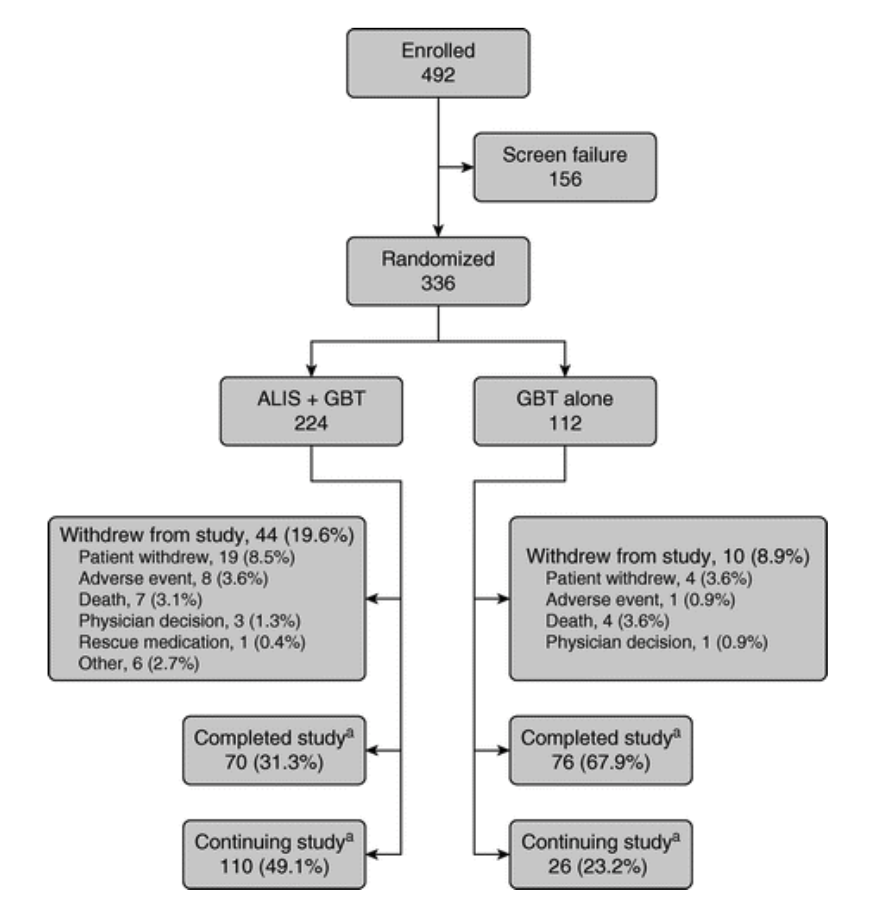
336例がランダマイズされ、2:1で割り付けられています。2:1の割付がされてる時点で、ALIS群に割付されなかった患者に不利益が起こるという前提なので、比較的強気なデザインが組まれています。
患者は北米、アジア、ヨーロッパの18カ国127の医療機関で実施。米国で141人、日本からは48人の患者が登録され、米国および日本が最大の貢献者と論文中に称されています。
主要評価項目は、Culture conversionと言うもので、恐らく培養変換と訳されると思いますが、
培養変換を治療後6ヶ月までに3回連続して毎月MAC菌が陰性で培養された患者の割合

副次評価項目は、6ヶ月時点で6分間の歩行試験で達成された距離が、ベースラインからの変化となっています。
これは上述した標準治療を行なった際にも用いられる指標となり、ALIS上乗せ群は治療後6ヶ月までに培養転換を達成し、6ヶ月時点で培養陰性だった患者はそのまま試験を継続し、最初の陰性培養から合計12ヶ月で治療を完了します。(なので合計16ヶ月の治療になる)そして治療段階の完了後、患者はフォローアップのためさらに12ヶ月間研究に残ったままになります。
※この論文が登録されたのが2018年9月なのでやはりまだ最終解析が出てないんでしょうね。
こちらがその結果になります。
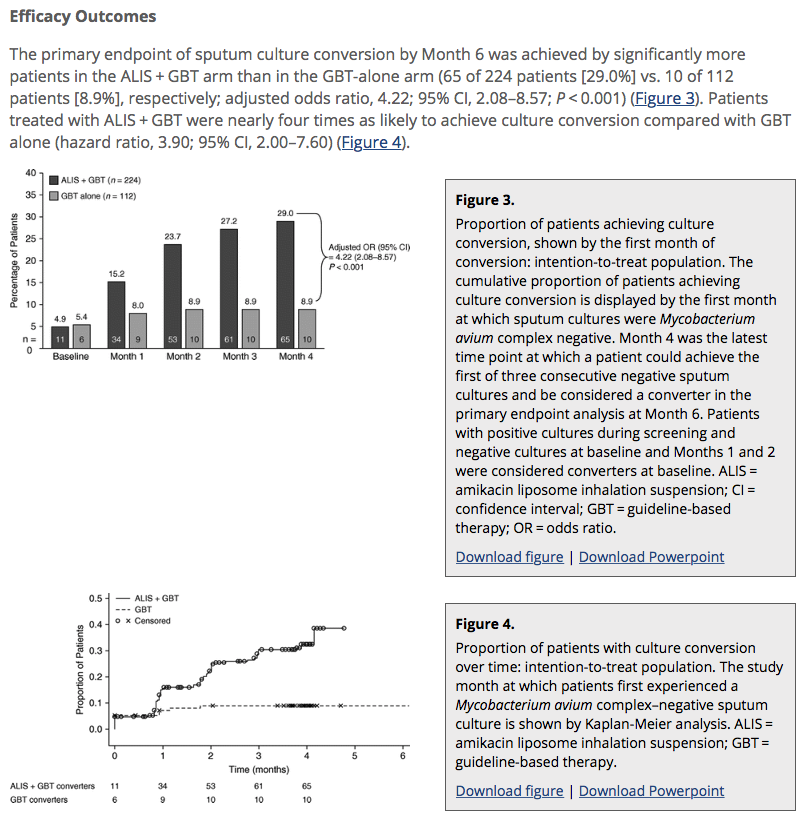
主要評価である6ヶ月目までの培養転換の割合は、ALIS上乗せ群が単独群と比較して有意に高かった。 (65 of 224 patients [29.0%] vs. 10 of 112 patients [8.9%], respectively; adjusted odds ratio, 4.22; 95% CI, 2.08–8.57; P < 0.001)
Figure3がそれを示していますが、表で見るととてもインパクトのある結果ですね。。
こちらが副次評価の歩行の部分
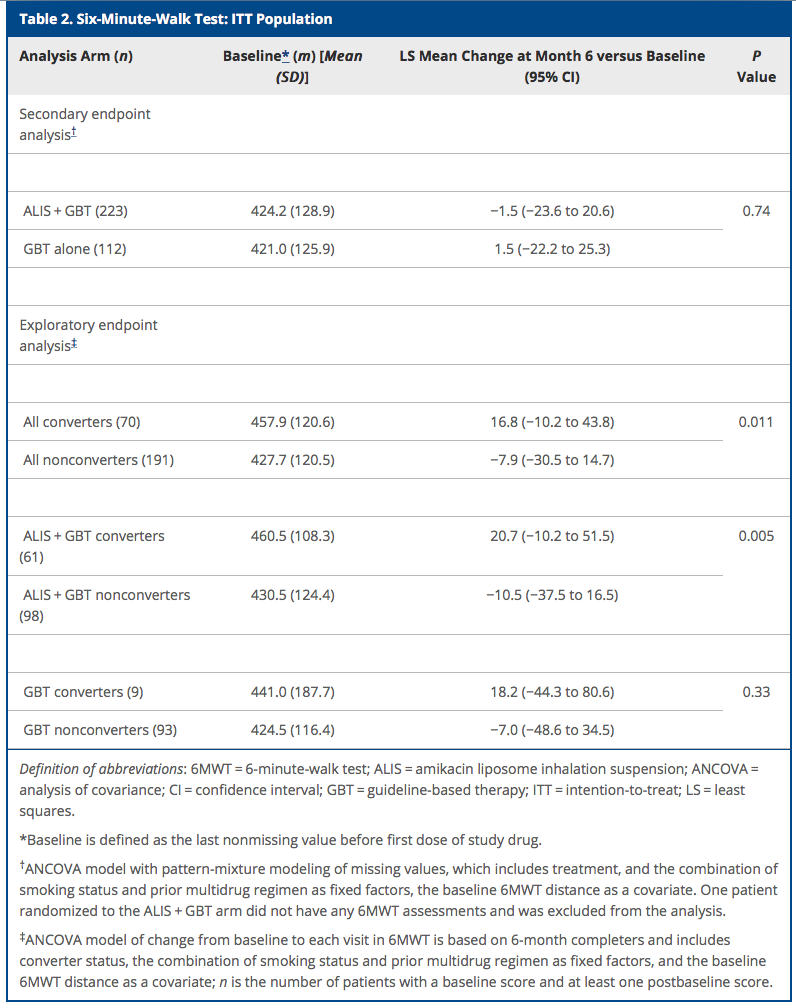
副次評価に関しては有意差は出ませんでした。
ただ、治験全体で事前に定義された探索的分析の中では、培養転換を伴った患者はそうでない患者よりも歩行に関して(論文の中では6MWTと表記)大幅な改善を示しました。
ここに関しては僕はAuthorの意図がよくわかってませんが、歩行に関しては全体で有意差は出てないが、培養転換ができた人は全員改善できている、でも2:1で割り付けられているためGBT単独群のサンプル数が足りない的な言い訳文書が書かれていますが、とにかく副次評価はネガティブです。
こちら安全性です。
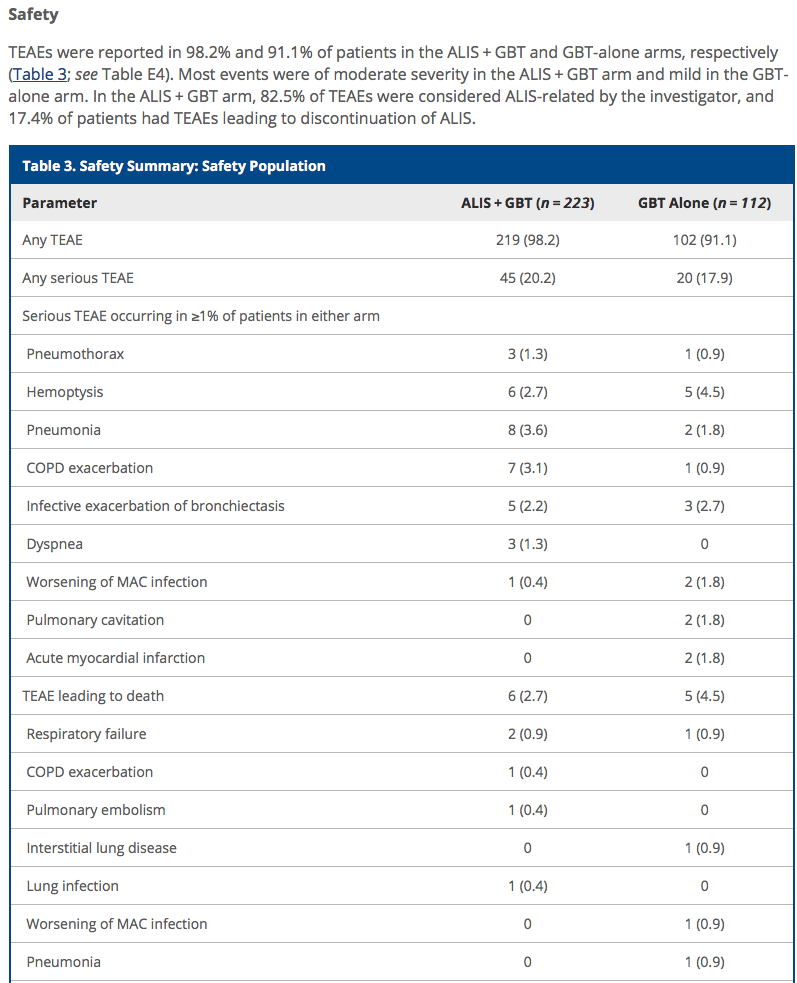
画像は途中までです。
ALIS併用群で98.2%、単独群で91.1%のAEが報告されています。
ALIS群では中程度の重症度、単独群では軽度でありました。
ただ、ALIS併用群の副作用の82.5%がALIS由来で、患者の17.4%がALIS投与によって中止に至ったと記載されてます。(この17.4%という数値は抗がん剤の試験だったら結構多い数字ですが、どうなんでしょうか)
一般的な副作用は呼吸器系イベント、発声障害、咳、喀血、呼吸困難、疲労、下痢、悪心、口腔咽頭痛で、いずれもALIS併用群のほうが高い傾向にあります。
抗がん剤ほどではないですが、抗生剤の組み合わせというのも結構ヘビーな治療なんですね。
ALIS群ではアミカシンの静注で懸念されている腎毒性などはほとんど発生してないので、改善されていると考えて良いのかと思います。
最後にディスカッション
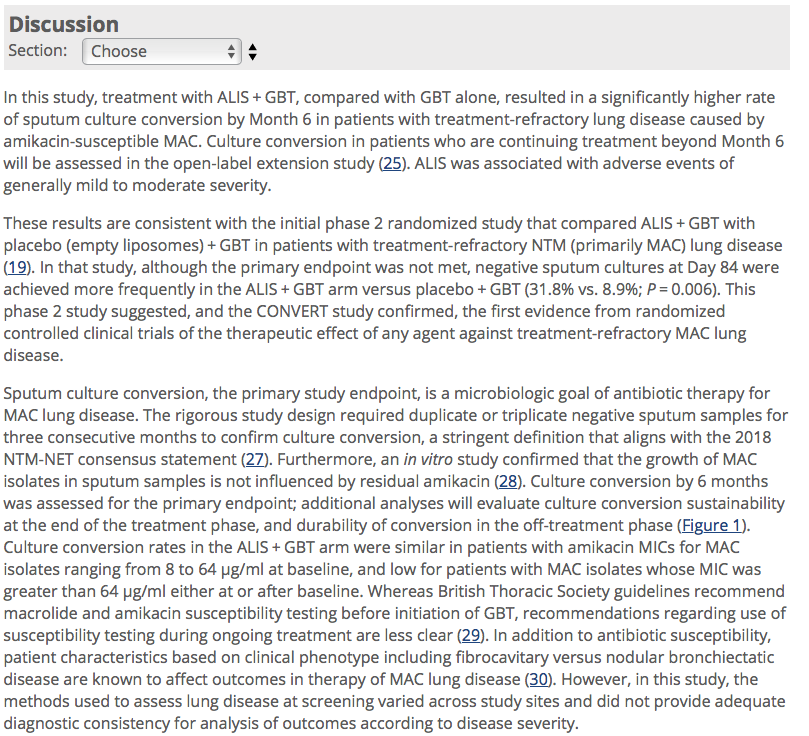
特筆すべきこととしては、このCONVERT試験の前段階で行われたP2試験では、ALIS群が単独群と比較して(31.8%vs8.9%)であった結果と、P3の今回の試験の結果(29%vs8.9%)が類似しており、再現性がある事。
歩行訓練のネガティブ結果に関しては、有意差は出なかったが、全体において、培養転換の無い患者の悪化に対して、培養転換のある患者で優位な改善が観察された。(要はセカンダリーはネガティブだけど、MAC菌陰性を達成してる患者は歩けるようになるから、とにかくMAC陰性を目指せるALISは良いという事を言いたいんだと思います。)※ナイスな言い訳だと思います!
それ以外は薬物動態や、アリケイスの血中濃度などが記載されています。
Arikayceは売れるのか?②
長くなりましたがアリケイスは売れるのか?というところで、
このP3論文を読んだら長くMRをやられている方は、
売れるだろうなぁって感じがするんではないかと思います。
アンメットニーズ度が高い疾患で、これだけ培養陰性率を達成していて、
報告論文もほぼ完璧にDTLできるレベルで、成功への道筋が描けると思います。
また、承認されてからの米国の医師の口コミや、評価をみていると、
現状、肺MAC症治療で、
アリケイス以外に強力な抗生物質を見つけるのは困難である事や、
できればもっと前段階で使用したいというコメントがありました。(治験実施中)
なので有効性に関してはアリケイスは標準治療よりはやはり優れていると言えます。
また、日本から48人の患者登録がされていて最大の功労者と評されている部分は注目で、
日本というのはご存知の通り非常に手厚い医療制度が敷かれている国です。
まだ有効性、安全性が確認されてない未知の薬剤の治験に入るリスクを取らなくても、
標準治療が当たり前のように受けられる環境であるにも関わらず、
未承認の治験に入る人がこの日本でこれだけ多いというのは、
治験を実施する医師がこの薬を高く評価している証拠なのかなと感じます。
副作用に関しては標準治療と比べると強いと言えると思うんですが、
元々の静注よりは改善されているという部分がこの会社の技術だと思いました。
Insmedの将来性
こちらInsmedのパイプラインになります。
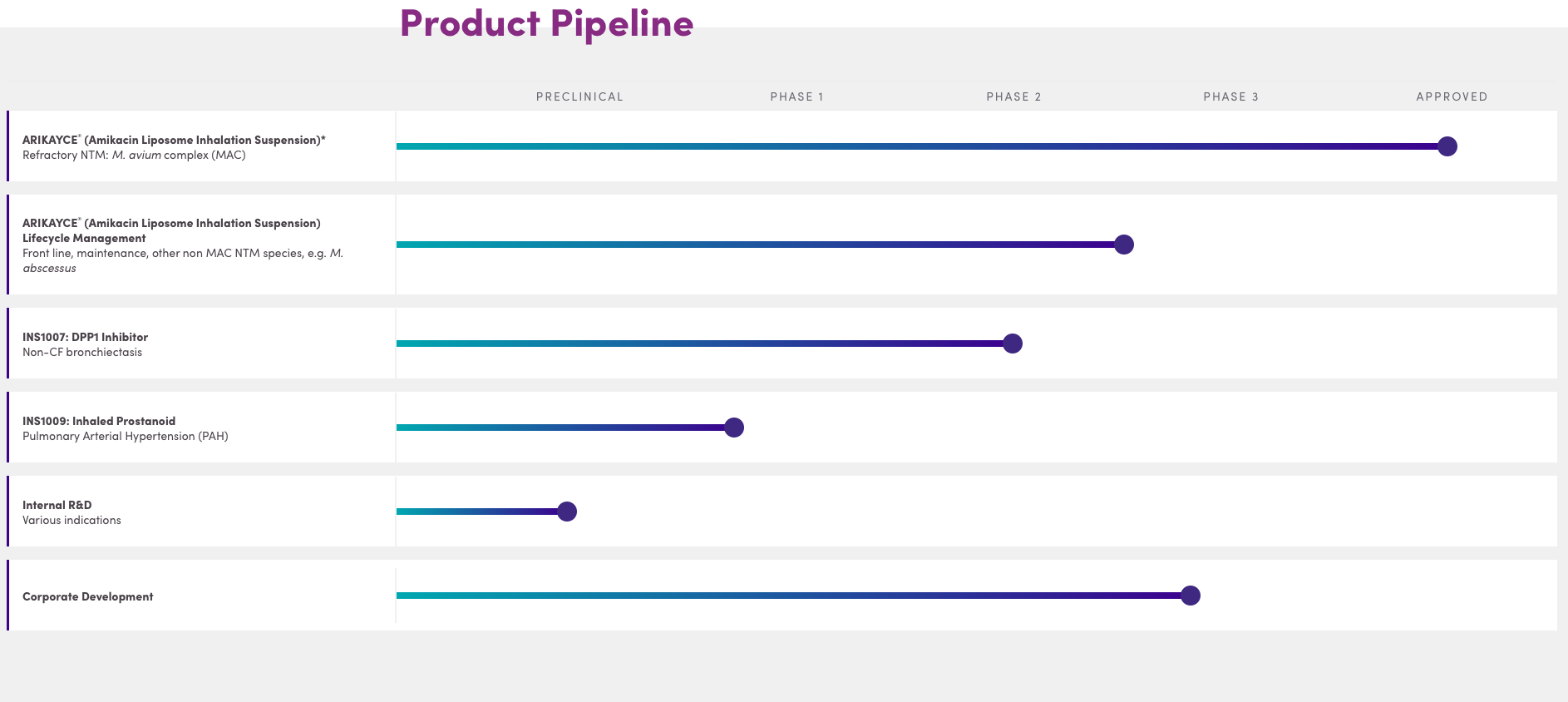
アリケイスは難治性の肺MACに上市後、当然ですがフロントラインの試験が行われています。
あとはアリケイスに関しては、メンテナンス(多分フロントラインでMAC陰性後の地固め的治療)、非MAC、NTM、膿瘍に対して行われています。
アリケイス以外には、
INS1007:非嚢胞性線維症気管支拡張症(NCFB)という疾患に対するDPP1 inhibitor、
INS1009:肺高血圧(PAH)、
この辺が主流になりそうですが、当面はアリケイスに注力していくと思います。
最後に
アメリカの会社で立ち上げてくる会社ってやっぱ魅力だと思います。
僕ももう少し若ければ挑戦したい会社です。
パイプラインも、いずれも呼吸器系路線なので、明確でわかりやすくて良いですね。
アリケイスも副作用など懸念点はありますが、
そこを凌駕する有効性、また日本から治験に多く参加しているというのは、
上市後もやりやすいのではないかと思います。
メディカル系やサプライチェーンの募集も人数が少ないので、
営業部門もそこまで多い人数ではないと予想してますが、
ご興味ある方是非頑張ってください!
案件はランスタッドが持っていますが、

ランスタッドってご存知ないかもしれませんが、
実はグローバルでは、リクルートも足元に及ばないくらい大きい会社で、
世界第2位の外資系転職エージェントになります。
日本ではヘルスケア部門に一番力を入れていて、
僕も1年くらい前に登録したんですが、希少な案件をサクッと紹介してくれるので、
結構おすすめです。
久しぶりに長い記事を書いたので疲れてしまいましたが、
僕自身とても勉強になりました。
ではまた!



コメント